De Acqua Expert – Em dezembro de 2023.
Introdução
O nitrogênio é um macronutriente essencial, cuja especiação e disponibilidade são conhecidas por impactar ambientes terrestres, de água doce e marinhos (Vitousek et al., 1997). Antes da Revolução Industrial, a conversão do gás N2 (nitrogênio não reativo) para formas reativas (formas que apoiam diretamente ou indiretamente o crescimento biológico) era principalmente realizada pela fixação biológica de N2 mediada por bactérias e arqueias (Galloway et al., 2004). Desde a Revolução Industrial, estima-se que a produção e descarga antropogênica de N reativo no meio ambiente tenha aumentado de 15 Tg/ano na década de 1860 para aproximadamente 259 Tg/ano em 2011. Esse aumento foi em grande parte impulsionado pela produção de alimentos e energia (Penuelas, 2012). Embora o metabolismo humano processe apenas cerca de 5% do pool global de N reativo, uma grande fração do N metabolizado está associada a descargas em estuários sensíveis e águas costeiras (Larsen et al., 2007). O acúmulo localizado de espécies de N reativo tem sido associado a problemas de poluição da água (Gruber & Galloway, 2008), os quais estão listados abaixo:
⦁ Concentrações da ordem de 3 mg/L de amônia (NH3) são tóxicas para peixes.
⦁ A amônia impacta na demanda de oxigênio dos cursos naturais de água por conta da proliferação de bactérias nitrificantes que utilizarão oxigênio dissolvido para oxidar a amônia a nitrito e nitrato. A redução da concentração de oxigênio dissolvido é prejudicial à vida de peixes e outras espécies aquáticas;
⦁ Excesso de nitrogênio pode causar eutrofização no corpo receptor, o que significa proliferação de algas e de outras plantas aquáticas;
⦁ Excesso de nitrato – NO3 (acima de 10 mg/L) em água potável pode causar uma doença denominada metemoglobinemia, distúrbio sanguíneo que impacta a capacidade do sangue de transportar oxigênio em crianças;
⦁ Cloraminas são compostos formados pela reação entre cloro e amônia, o que pode ser comum no sistema de desinfecção de ETEs. As cloraminas, além de serem prejudiciais à saúde, diminuem a eficiência da desinfecção do efluente.
Dito tudo isso, o tratamento dos efluentes sanitários e industriais antes da descarga nos corpos d’água continua a ser uma estratégia eficaz para remover diretamente a fração de N reativo associada ao metabolismo humano. Este artigo faz uma revisão das formas mais utilizadas de remover N e apresenta os desafios de cada tecnologia.
N em esgoto doméstico
Dos nutrientes excretados pelos seres humanos, de 85 a 90% do nitrogênio reativo pode ser encontrado na urina, enquanto o restante está associado às fezes (Larsen & Gujer, 1996). O nitrogênio excretado está principalmente na forma de amônia/amônio ou nitrogênio organicamente ligado (N orgânico). O teor de nitrogênio de águas residuais domésticas também é influenciado por resíduos de alimentos descartados diretamente no esgoto e por produtos de cuidado pessoal comerciais. Como a dieta e o consumo de água variam de lugar para lugar, a concentração de nitrogênio em esgotos domésticos pode variar de 20 a 150 mg N/L, sendo as concentrações mais baixas associadas a regiões que têm acesso mais fácil ao abastecimento de água potável.
O nitrogênio em águas residuais domésticas é em grande parte biodisponível (Figura 1) e pode estimular a eutrofização em águas costeiras e estuários se não for tratado antes do descarte (Howarth & Marino, 2006). Consequentemente, o tratamento de efluentes evoluiu para abordar a remoção tanto de nitrogênio quanto de fósforo para ajudar a limitar a produção primária. Embora o nitrogênio possa ser removido dos efluentes por meios físico-químicos e biológicos, os processos de lodos ativados tornaram-se a abordagem mais comumente aplicada para remover o nitrogênio dos efluentes.
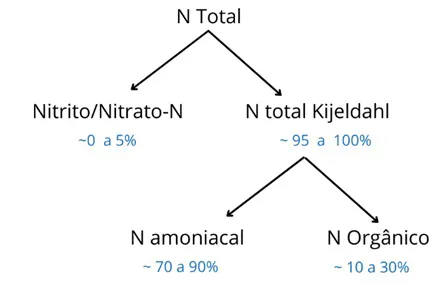
Figura 1: Especificação do N em Esgoto Doméstico.
Formas de Remoção de N
A forma mais comum e conhecida de remoção de nitrogênio é por assimilação.
O nitrogênio é assimilado pelas bactérias principalmente para a síntese de compostos celulares, tais como proteínas e ácidos nucleicos (DNA e RNA), isso significa que o N é um componente essencial dessas macromoléculas biológicas, desempenhando um papel crucial no crescimento e na reprodução das bactérias dentro do lodo ativado.
De forma bem resumida, o lodo excedente (descartado) contém em sua composição cerca de 12% de nitrogênio total, que foi assimilado e retirado do liquor contido no reator biológico.
Assim, o cálculo mais rudimentar que existe é justamente o cálculo da assimilação de amônia na ETE, contabilizada como Nitrogênio Total Kjeldahl (NTK): A fração de amônia no lodo excedente descartado corresponde a 0,12 kg NTK/kg SSV.
As outras formas de remoção de nitrogênio dos despejos líquidos são pelos processos de nitrificação e desnitrificação.
Nitrificação
Nitrificação é o termo usado para descrever a primeira etapa do processo de remoção biológica de nitrogênio, em que a amônia é oxidada a nitrito e o nitrito é oxidado a nitrato (Metcalf & Eddy, 2014). Esse processo é realizado por bactérias quimiossintetizantes nitrificantes aeróbias, que utilizam os compostos nitrogenados inorgânicos como fonte de energia, carbono inorgânico (CO2) como fonte de carbono e o oxigênio (O2) como aceptor final de elétrons.
A Nitrificação ocorre em dois estágios, sendo o primeiro deles a conversão da amônia (NH3) em nitrito (NO2-). Esta reação é realizada pelas enzimas amônia monooxigenase e na sequência pela hidroxilamina oxidorredutase, gerando assim o nitrito (Equação 1). As principais bactérias oxidantes de amônia são as dos gêneros Nitrosomonas, Nitrosovibrio, Nitrosococcus, Nitrolobus e Nitrospira.
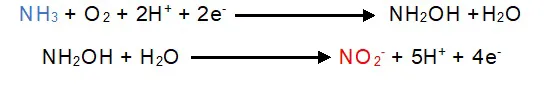
Equação 1: Processo resumido da primeira etapa da nitrificação.
No segundo estágio, as bactérias dos gêneros Nitrobacter, Nitrococcus e Nitrospira oxidam a molécula de nitrito (NO2-), produzindo assim o nitrato (NO3-), através da atividade da enzima nitrito oxidorredutase.

Equação 2: Processo resumido da segunda etapa da nitrificação.
A Figura 2 apresenta uma colônia de bactérias nitrificantes registrada em um sistema de lodos ativados por aeração prolongada. Esta micrografia foi feita utilizando objetiva de 10 x com contraste de fase.
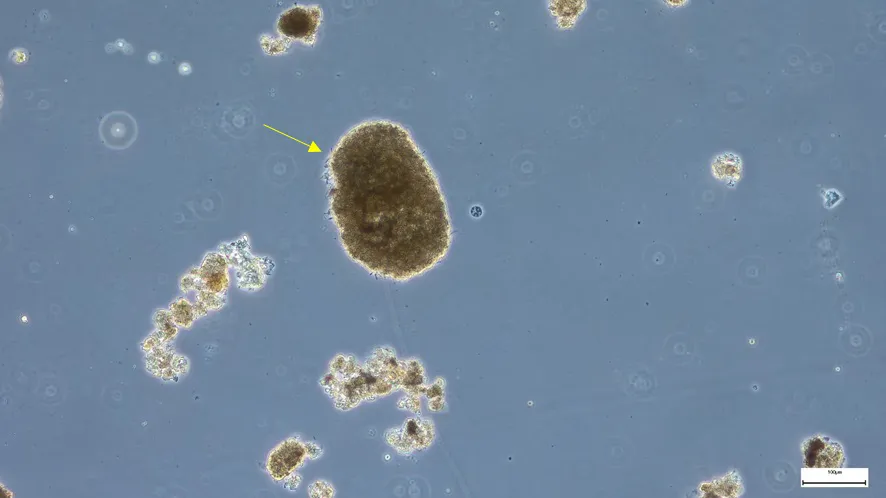
Figura 2: Colônia de bactérias nitrificantes. In vivo. 100 x. Contraste de fase.
Fonte: Acqua Expert.
Na etapa de nitrifricação os seguintes fatos devem ser observados com atenção:
⦁ A 1ª etapa da reação de nitrificação demanda muito oxigênio, para ser mais exato, a oxidação de 1 mg consome 4,57 . De acordo com a EPA (2002) a concentração de OD deve ser mantida no reator aeróbio acima de 2,0 mg para assegurar que as reações de nitrificação não cessem, já que as bactérias nitrificantes têm baixa capacidade de armazenamento de energia;
⦁ A nitrificação libera íons H+, consumindo alcalinidade e podendo reduzir o pH ao longo do tanque de aeração. O consumo de alcalinidade é de 7,14 . Esse decréscimo pode ser controlado pela alcalinidade, sendo importante a manutenção de uma faixa variando entre 6,5 e 8,0 (EPA, 2002).
⦁ A taxa de crescimento da Nitrosomonas é bem lenta em relação às bactérias envolvidas na remoção carbonácea. Por causa disso, a idade do lodo de sistemas onde há nitrificação deve ser mantida mais elevada.
Desnitrificação
Desnitrificação, por sua vez, é o termo usado para descrever a segunda etapa do processo de remoção biológica de nitrogênio, em que o nitrato é oxidado a nitrogênio gasoso (Metcalf & Eddy, 2014). Neste processo as bactérias utilizam o oxigênio contido no nitrato para metabolizar carbono orgânico. Ao contrário da nitrificação, o processo de desnitrificação envolve uma gama elevada de bactérias heterotróficas, muitas delas inclusive são comumente encontradas em sistemas típicos de tratamento biológico que não demandem remoção de nitrogênio (WEF, 2005). Estes organismos são comuns porque são facultativos e podem usar tanto o oxigênio livre quanto o nitrato como fonte de energia. Os gêneros mais comuns são: Hyphomicrobium, Acidovorax, Azoarcus/Thauera complexo, Curvibacter, Dechloromonas, Rhodobacter, Zoogloea.
O processo de desnitrificação pode ser representado pela Equação 3:

Equação 3: Processo resumido da desnitrificação.
A Figura 3 apresenta algumas bactérias desnitrificantes da espécie Hyphomicrobium sp. registradas em um sistema de lodos ativados por aeração prolongada. Esta micrografia foi feita utilizando objetiva de 100 x com contraste de fase e óleo de imersão
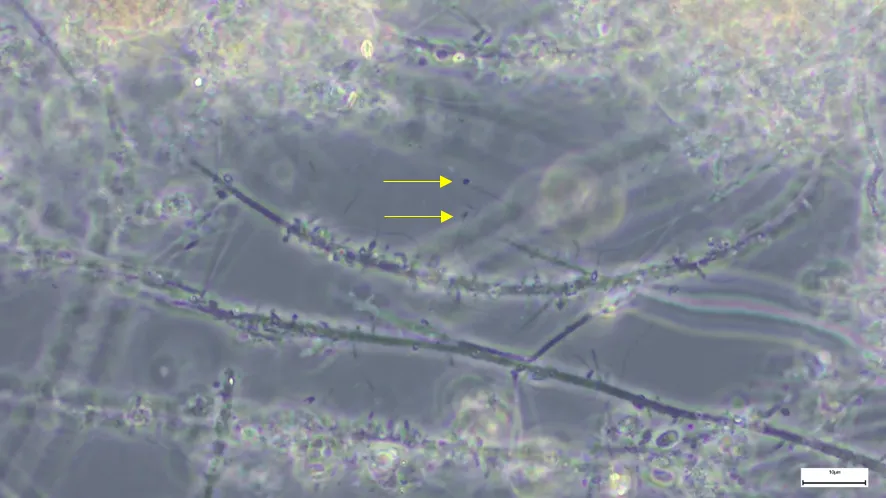
Figura 3: Bactéria da espécie Hyphomicrobium sp. In vivo. 1000 x. Contraste de fase.
Fonte: Acqua Expert.
Processos tradicionais que fazem remoção biológica de N.
Para ter uma boa remoção de Nitrogênio do efluente é necessário então implantar um sistema biológico que estimule os processos de nitrificação e desnitrificação. Mas, como ficou claro na sessão anterior, não existe desnitrificação sem que aconteça a nitrificação antes.
Os três processos de remoção de N mais empregados no Brasil são:
⦁ Lodo Ativado com Pré-Desntirificação
⦁ Lodo Ativado com Pós-Desnitirificação e
⦁ Sistema Bardenpho
Segue abaixo uma descrição mais detalhada de cada um.
Pré-Desnitrificação
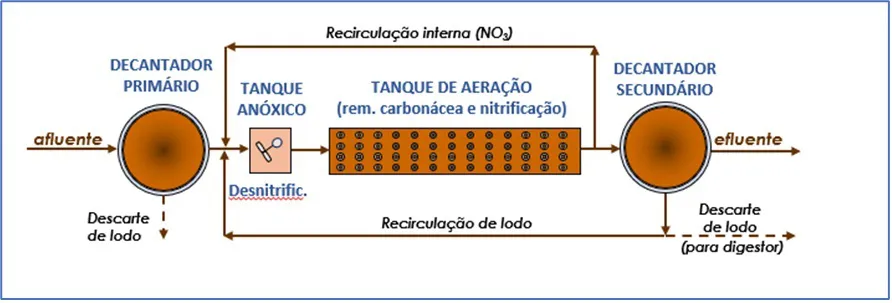
É o processo mais empregado no Brasil para desnitrificação, sendo seu fluxograma apresentado na Figura 4.
O reator possui uma zona anóxica inicial seguida por uma zona aeróbia. O processo de nitrificação ocorre na zona aeróbia formando o nitrato, e por meio de recirculação interna são redirecionados à câmara anóxica. Essa recirculação interna é realizada com altas razões de recirculação, que podem variar entre 100% e 400% da vazão afluente. Quando na zona anóxica, as bactérias desnitrificantes irão transformar o nitrato em nitrogênio gasoso e energia, como já apresentado.
É importante destacar que 3 mg DBO5/L são removidas a cada 1 mg NO3-N/L desnitrificada. Isso significa que o esgoto recirculado deverá ter relação DBO/NO3-N superior à indicada acima para possibilitar a desnitrificação.
Esse arranjo apresenta algumas vantagens interessantes, como redução no tempo de detenção na zona anóxica em comparação com outro arranjo, o de pós- desnitrificação; outra vantagem é a redução no consumo de oxigênio no tanque de aeração devido a estabilização da matéria orgânica que já ocorre na zona anóxica; também pode ser levada em consideração a redução do volume da zona aeróbia uma vez que já haverá uma boa estabilização da DBO na zona anterior e por fim há economia em relação aos equipamentos quando comparada com a pós-desnitrificação.
Como desvantagens é importante ressaltar que o reciclo garante que 75 a 90% do nitrato disponível seja recirculado para a zona anóxica, limitando o potencial de desnitrificação. Além disso, há a possibilidade de transferência de oxigênio do tanque aeróbio podendo reduzir a eficiência de remoção pelos organismos desnitrificantes.
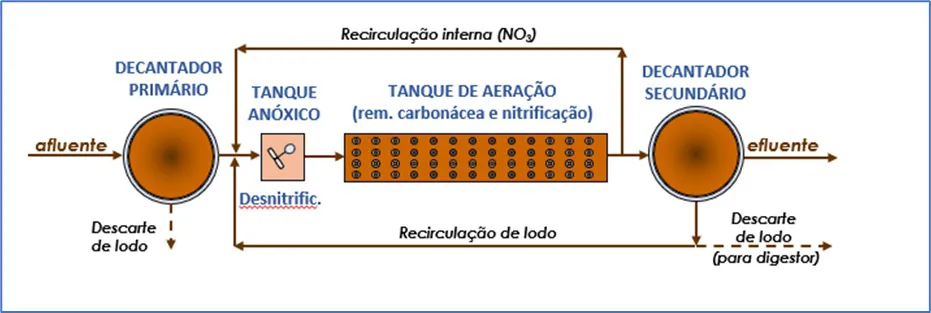
Figura 4: Fluxograma de ETE com pré-desnitrificação
Pós-Desnitrificação
Neste arranjo. o tanque aeróbio precede a câmara anóxica, como na configuração padrão para remoção de carbono, a diferença está no fato desse processo ter uma zona aeróbia final após a zona anóxica. Essa conformação faz com que a taxa de eliminação do nitrogênio não seja mais dependente da recirculação, conforme representado abaixo na Figura 5.
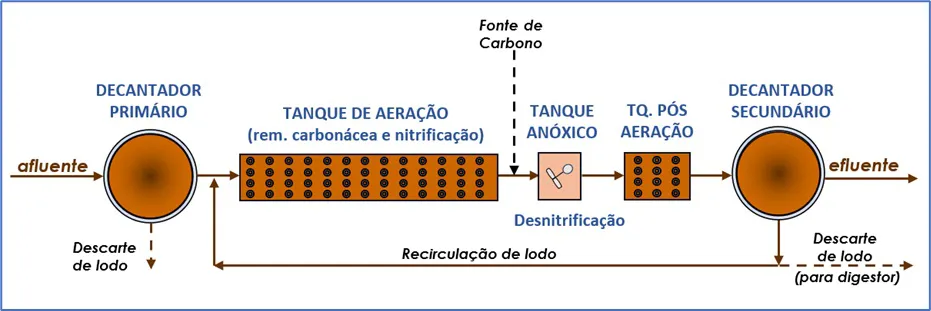
Figura 5: Fluxograma de ETE com pós desnitrificação.
A remoção de carbono e produção de nitrato ocorrem na zona aeróbia. Os nitratos entram na zona anóxica onde são reduzidos a nitrogênio gasoso e deixa o sistema, caracterizando a não necessidade de recirculações internas.
Como maior desvantagem podemos citar que grande parte da matéria orgânica é degradada no tanque aeróbio, o que implica em baixas quantidades para serem utilizadas pelas bactérias desnitrificantes. Esse fato gera a possibilidade de as taxas de desnitrificação serem limitadas pela quantidade de carbono orgânico disponível (DBO). Uma prática muito comum para evitar tal problema, e que é amplamente utilizada, é a introdução de uma fonte de carbono no tanque anóxico, como por exemplo: etanol, glicerol e açúcar. Porém essa dosagem deve ser muito bem controlada ou então pode haver aumento na quantidade de matéria orgânica presente no efluente final.
Sistema Bardenpho
Esse processo consiste em uma combinação dos dois arranjos, pré-desnitrificação e pós-desnitrificação, além da zona de reaeração final. Esse sistema nos traz uma eficiência de remoção de nitrogênio da ordem de 90%, uma vez que os nitratos não removidos na primeira zona anóxica podem ser removidos na posterior Figura 6).
Devido a sua configuração, esse sistema precisa de um tempo de detenção maior no tanque de aeração para que a nitrificação possa ocorrer. Isso implica na necessidade de que os reatores tenham volume total maior, acarretando maiores investimentos.
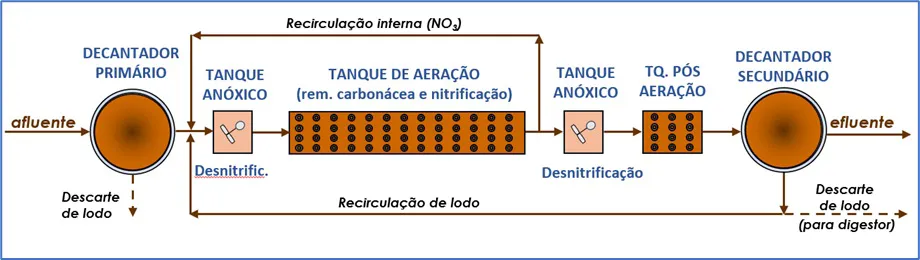
Figura 6: Fluxograma de ETE com pré e pós desnitrificação – Sistema Bardenpho
Nitrificação e Desnitrificação Simultâneas (NDS)
Os processos biológicos baseados em biomassa suspensa, como vistos na sessão anterior, são eficazes na remoção de carbono orgânico e nutrientes de efluentes domésticos. No entanto, essa tecnologia é limitada por alguns problemas, como a capacidade de sedimentação do lodo, exigindo grandes reatores, decantadores e recirculação do lodo (Luostarinen et al, 2006 e Pastorelli, 1999).
Por outro lado, os processos biológicos com biofilme têm se mostrado confiáveis na redução de carga orgânicas e nutrientes, sem alguns dos problemas dos processos de lodo ativado (Odegaard et al, 1994 e Rahimi et al, 2001).
O reator de biofilme de leito móvel (MBBR – Figura 7) é uma alternativa muito eficiente para remoção de carbono orgânico e nitrogênio, combinando as vantagens do processo de lodo ativado e de um reator de biofilme, incorporando suportes flutuantes que proporcionam uma grande área superficial para colonização dos microrganismos, sem a necessidade de reciclo do lodo [Mc Quarrie e Boltz, 2011, Rusten et al, 2006 e Jahren, et al, 2002) (Figura 8).
Outras vantagens do MBBR incluem a redução no espaço em comparação com o sistema tradicional de lodo ativado, facilidade de atualização das instalações existentes, baixa perda de carga em comparação com configurações de filtro submerso, menos requisitos de limpeza ou retro lavagem, aumento do tempo de retenção de sólidos para organismos de crescimento lento, como é o caso das bactérias nitrificantes, e recuperação mais rápida de condições de sobrecarga (Khan et al, 2011 e Guo 2010).
Estudos recentes revelaram que no biofilme do sistema MBBR as etapas de Nitrificação e Desnitrificação podem ocorrer simultaneamente no mesmo reator, este processo é denominado nitrificação e desnitrificação simultâneas (NDS) (Gupta, 2001 e Foresti et al, 2009).
A NDS oferece várias vantagens em comparação com a remoção de nitrogênio por meio da nitrificação e desnitrificação convencionais:
⦁ não há necessidade de dois tanques separados operados em série ou aeração intermitente em um único tanque, permitindo assim a produção contínua de efluente em uma área menor;
⦁ utiliza menos carbono, cerca de 22–40%, o que reduz a produção de lodo em 30%;
⦁ requer menos alcalinidade, pois a alcalinidade é produzida durante a desnitrificação;
⦁ consome menos energia devido à menor necessidade de aeração.
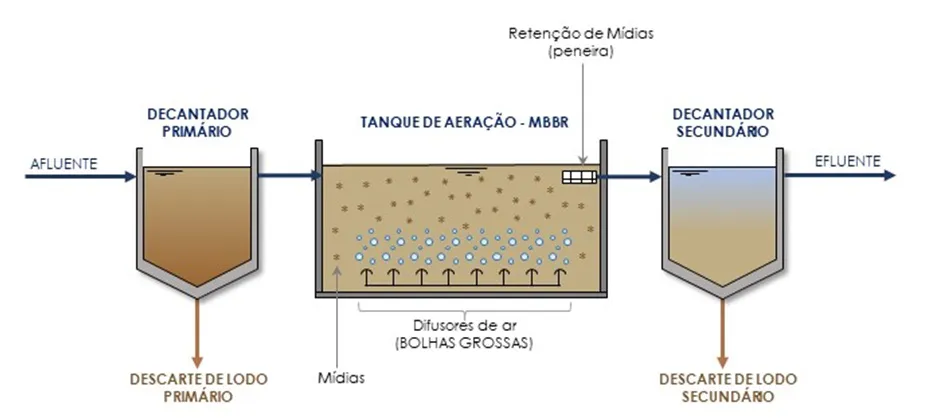
Figura 7: Fluxograma de um sistema MBBR.

Figura 8: Mídias de contato modelo MBBR 500 da B&F dias.
A NDS oferece várias vantagens em comparação com a remoção de nitrogênio por meio da nitrificação e desnitrificação convencionais:
Mais detalhes sobre como melhorar a nitrificação e desnitrificação na sua ETE assista nosso vídeo completo em: https://youtu.be/Bt-YyAef0jY.
Referências Bibliográficas
EPA (2002). AMERICAN WATER WORKS ASSOCIATION (AWWA). Nitrification.
Foresti E, Pozzi E, Chinalia F A, Daniel L M C. (2009). Removal of ammonium via simultaneous nitrification–denitrification nitrite-shortcutin a single packed bed batchreactor. Bioresour Technol.100:1100–7.
Galloway J. N., Dentener F. J., Capone D. G., Boyer E. W., Howarth R. W., Seitzinger S. P., Asner G. P., Cleveland C. P., Green P. A., Holland E. A., Karl D. M., Michaels A. F., Porter J. H., Townsend A. R. and Vöosmarty C. J. (2004). Nitrogen cycles: past, present, and future. Biogeochem., 70, 153–226
Gruber N. and Galloway J. N. (2008). An earth-system perspective of the global nitrogen cycle. Nature, 451(7176), 293–296.
Guo W S, Ngo HH, Dharmawan F, Palmer C G. (2010). Roles of polyurethane foam in aerobic Moving and fixed bed bioreactors. Bioresour Technol. 101:1435–9.
Gupta A B, Gupta S K. (2001). Simultaneous carbon and nitrogen removal from high strength domestic wastewater in anaerobic RBC biofilm. Water Res. 35:1714–22.
Howarth R. W. and Marino R. (2006). Nitrogen as the limiting nutrient for eutrophication in coastal marine ecosystems: evolving views over three decades. Limnol. Oceanog., 51(1), 364–376.
Jahren S J, Rintala J A, Odegaard H. (2002). Aerobic Moving bed biofilmreactor treating thermomechanical pulping White water under thermophilic conditions. Water Res. 36:1067–75.
Khan S J, Ilyas S, Javid S, Visvanathan C, Jegatheesan V. (2011). Performance of suspended and attached growth MBR systems intreating high strength synthetic wastewater. Bioresour Technol. 102:5331–6.
Larsen T. A., Maurer M., Udert K. M. and Lienert J. (2007). Nutrient cycles and resource management: implications for the choice of wastewater treatment technology. Water Sci. Technol., 56(5), 229–237.
Larsen, T. A. and Gujer W. (1996). Separate management of anthropogenic nutriente solutions (human urine). Water Sci. Technol., 34(3–4), 87–94.
Luostarinen S, Luste S, Valentin L, Rintala J. (2006). Nitrogen removal from on-site treated anaerobic efluente susing intermittently aerated Moving bed biofilmreactor satlow temperature.WaterRes. 40:1607–15.
Mc Quarrie JP ,Boltz JP. (2011). Moving bed biofilmreactor technology: process applications, design, and performance. Water Environ Res. 83:560–75.
Metcalf & Eddy. (2014) Tratamento de Efluentes e Recuperação de Recursos. 5. ed. Porto Alegre: Amgh, 2016. 2012 p.
Odegaard H, Rusten B, Westrum T. Anew. (1994) Moving bed biofilm reactor application sand results. WaterSci Technol. 29:157–65.
Odegaard H. (2006). Innovations in wastewater treatment: the Moving bed biofilm process. Water Sci Technol.53:17–33.
Pastorelli G, Canziani R, Pedrazzi L, Rozzi A. (1999). Phosphorus and nitrogen removalin moving-bed sequencing batch biofilm reactors. Water Sci Technol. 40:169–76.
Penuelas J., Sardans J., Rivas-Ubach A. and Janssens I. A. (2012). The human-induced imbalance between C, N and P in Earth’s life system. Global Change Biol., 18, 3–6.
Rahimi Y, Torabian A, Mehrdadi N, Habibi-Rezaie M, Pezeshk H, Nibi-Gidhendi GR. (2011). Optimizing aeration rates for minimizing membrane fouling and its effect on sludge characteristics in a Moving bed membrane bioreactor. J Hazard Mater.186:1097–102.
Rusten B, Eikebrokk B, Ulgenes Y, Lygren E. (2006). Designand operations of the Kaldnes Moving bed biofilmreactors. Aquacult Eng. 34:322–31.
Vitousek P. M., Aber J. D., Howarth R. W., Likens G. E., Matson P. A., Schindler D. W., Schlesinger W. H. and Tilman D. G. (1997).
Human alteration of the global nitrogen cycle: sources and consequences. Ecol. Applic., 7(3), 737–750.
WEF (1992). Design manual of wastewater treatment plants. Manual of Practice 8.